¿Con qué letra se representa el número atómico? Descubre la respuesta aquí
El número atómico es un concepto fundamental en química y física que determina la identidad de un elemento químico. Sin embargo, muchas personas se preguntan: ¿con qué letra se representa el número atómico? Esta consulta puede parecer sencilla, pero tiene implicaciones importantes en el estudio de la materia. En este artículo, exploraremos qué es el número atómico, cómo se representa y su relevancia en el contexto de la tabla periódica. Además, discutiremos ejemplos concretos de elementos y sus respectivos números atómicos, lo que te permitirá comprender mejor este concepto clave en la ciencia. Si alguna vez te has preguntado cómo se relacionan los elementos químicos con su número atómico, estás en el lugar adecuado. ¡Sigue leyendo para descubrirlo!
¿Qué es el número atómico?
El número atómico es un número entero que se asigna a cada elemento químico en la tabla periódica. Este número representa la cantidad de protones que se encuentran en el núcleo de un átomo de ese elemento. Por ejemplo, el hidrógeno, que es el primer elemento en la tabla periódica, tiene un número atómico de 1, lo que significa que posee un solo protón en su núcleo. Este concepto es crucial porque el número atómico determina no solo la identidad del elemento, sino también su posición en la tabla periódica.
Importancia del número atómico
El número atómico tiene varias funciones importantes en la química. En primer lugar, determina la configuración electrónica del átomo, lo que influye en sus propiedades químicas y en cómo interactúa con otros elementos. Además, el número atómico también se utiliza para identificar isótopos de un elemento. Por ejemplo, el carbono tiene un número atómico de 6, pero puede tener isótopos como el carbono-12 y el carbono-14, que difieren en el número de neutrones, aunque el número de protones permanece constante.
Relación con la tabla periódica
La tabla periódica está organizada en función del número atómico de los elementos. Cada elemento ocupa una posición específica que refleja su número atómico. Esto no solo facilita la identificación de los elementos, sino que también permite predecir su comportamiento químico. La organización de la tabla periódica en filas y columnas también se basa en el número atómico, donde los elementos en la misma columna comparten propiedades químicas similares.
¿Cómo se representa el número atómico?
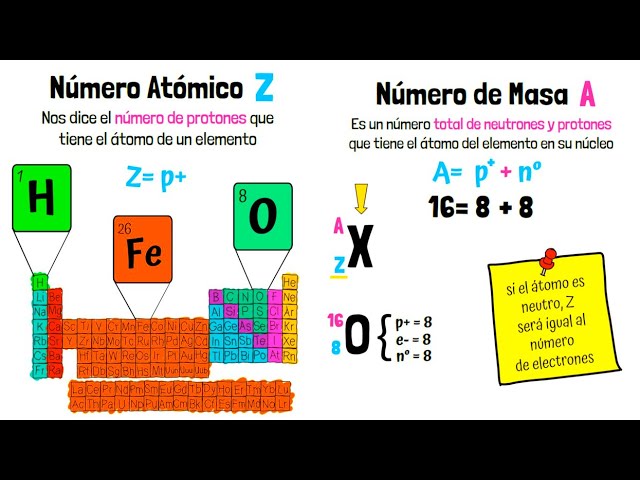
El número atómico se representa con la letra «Z». Esta letra proviene de la palabra alemana «Zahl», que significa «número». En la notación química, el número atómico se coloca como un subíndice a la izquierda del símbolo del elemento. Por ejemplo, el helio, que tiene un número atómico de 2, se representa como 2He. Esta notación es universalmente reconocida en la comunidad científica y permite una identificación clara y precisa de los elementos químicos.
Ejemplos de notación
Veamos algunos ejemplos de cómo se utiliza la letra «Z» para representar el número atómico de diferentes elementos:
- 1H: Hidrógeno
- 6C: Carbono
- 8O: Oxígeno
- 26Fe: Hierro
- 79Au: Oro
En cada uno de estos ejemplos, el número que precede al símbolo del elemento indica su número atómico. Esta representación es crucial para entender la composición y propiedades de cada elemento.
Otras notaciones relacionadas
Además del número atómico, es importante mencionar otras notaciones relacionadas que pueden causar confusión. Por ejemplo, el número de masa, que se representa con la letra «A», se refiere a la suma de protones y neutrones en el núcleo de un átomo. En la notación química, el número de masa se coloca como un superíndice a la izquierda del símbolo del elemento. Por ejemplo, el carbono-12 se representa como 12C, donde 12 es el número de masa. Esta diferenciación es esencial para comprender la estructura del átomo y sus isótopos.
El número atómico en la práctica
El número atómico no solo es un concepto teórico, sino que tiene aplicaciones prácticas en diversas áreas. Desde la química hasta la medicina, el número atómico juega un papel fundamental en la identificación y manipulación de elementos y compuestos. Por ejemplo, en la medicina nuclear, se utilizan isótopos radiactivos de elementos con diferentes números atómicos para diagnósticos y tratamientos. El yodo-131, que tiene un número atómico de 53, se utiliza en el tratamiento de enfermedades de la tiroides.
Aplicaciones en la industria
En la industria, el conocimiento del número atómico es esencial para la producción de materiales y compuestos. Por ejemplo, los ingenieros químicos deben entender cómo las propiedades de los elementos, determinadas por su número atómico, afectan las reacciones químicas y la formación de compuestos. Esto es crucial en la fabricación de productos farmacéuticos, plásticos y otros materiales. Además, el número atómico también es fundamental en la investigación de nuevos materiales, donde los científicos experimentan con diferentes combinaciones de elementos para crear compuestos innovadores.
Investigación y desarrollo
La investigación en el campo de la física y la química también se beneficia del estudio del número atómico. Los científicos utilizan el número atómico para clasificar elementos en la búsqueda de nuevos materiales y para comprender fenómenos a nivel subatómico. Esto incluye la exploración de nuevas fuentes de energía, como la fusión nuclear, donde el número atómico juega un papel crucial en la comprensión de cómo los núcleos atómicos interactúan entre sí.
Preguntas Frecuentes (FAQ)
¿Qué es el número atómico y cómo se utiliza?
El número atómico es la cantidad de protones en el núcleo de un átomo y se representa con la letra «Z». Se utiliza para identificar elementos en la tabla periódica y determina sus propiedades químicas. Cada elemento tiene un número atómico único, lo que lo diferencia de otros elementos. Por ejemplo, el oxígeno tiene un número atómico de 8, lo que significa que tiene 8 protones en su núcleo.
¿Por qué es importante el número atómico?
El número atómico es crucial porque determina la identidad de un elemento y sus propiedades químicas. Influye en cómo los elementos interactúan entre sí y en cómo se comportan en reacciones químicas. Además, es fundamental para clasificar elementos en la tabla periódica, lo que facilita su estudio y comprensión.
¿Cómo se relaciona el número atómico con el número de masa?
El número atómico (Z) representa la cantidad de protones en el núcleo, mientras que el número de masa (A) es la suma de protones y neutrones. Por lo tanto, el número de masa puede variar entre isótopos de un mismo elemento, que tienen el mismo número atómico pero diferentes cantidades de neutrones. Por ejemplo, el carbono-12 y el carbono-14 tienen el mismo número atómico (6), pero diferentes números de masa (12 y 14, respectivamente).
¿Todos los elementos tienen un número atómico?
Sí, todos los elementos químicos tienen un número atómico. Este número es una característica fundamental que define la naturaleza del elemento. Desde el hidrógeno, con un número atómico de 1, hasta elementos más pesados como el uranio, con un número atómico de 92, cada elemento tiene un número atómico único que lo identifica en la tabla periódica.
¿Cómo se determina el número atómico de un elemento?
El número atómico de un elemento se determina mediante experimentos que cuentan la cantidad de protones en el núcleo de sus átomos. Esta información se utiliza para organizar los elementos en la tabla periódica. La identificación del número atómico es esencial en química y física, ya que proporciona una base para entender la estructura y el comportamiento de los elementos.
¿Qué pasa si un elemento tiene un número atómico diferente?
Si un elemento tiene un número atómico diferente, significa que se trata de un elemento diferente. Cada número atómico corresponde a un elemento específico en la tabla periódica. Por ejemplo, el oxígeno (Z=8) no puede convertirse en nitrógeno (Z=7) simplemente cambiando el número de protones, ya que esto alteraría su identidad como elemento químico.
¿Cómo se utiliza el número atómico en la química orgánica?
En química orgánica, el número atómico se utiliza para entender la estructura y reactividad de compuestos orgánicos. Conocer el número atómico de los elementos que componen una molécula ayuda a predecir cómo reaccionarán en diferentes condiciones. Por ejemplo, los átomos de carbono (Z=6) son fundamentales en la formación de enlaces químicos, lo que permite la creación de estructuras complejas como proteínas y ácidos nucleicos.